血小板減少症という名前はあくまでも症状を表すものであり、血小板が減少した原因を表しているわけではありません。一般的に、血小板が減少する理由で多いのは、自ら作った抗体で血小板を壊してしまう特発性血小板減少性紫斑病だと言われています。また、解熱鎮痛薬いより血小板などが減少することもあるので、そうした薬が原因となっている可能性もあるかもしれません。いずれにせよ、血液内科などの、専門医に診断をしてもらうことが大切です。
| 疾病名 | 主な症状 |
| 特発性血小板減少性紫斑病 | 明らかな病気や薬剤の服薬がなく血小板数が減少し、出血しやすくなる病気です。血小板数が10万/μL未満に減少した場合、この病気が疑われます。病気が起こってから6ヶ月以内に血小板数が正常に回復する「急性型」は小児に多く、6ヶ月以上血小板減少が持続する「慢性型」は成人に多い傾向にあります。 |
血小板は、出血をとめるために非常に大切な細胞です。ですから、この数が減ると出血し易くなり、また出血が止まりにくくなり、次のような種々の程度の出血症状がみられます。
・点状や斑状の皮膚にみられる出血
・歯ぐきからの出血、口腔粘膜出血、鼻血
・便に血が混じったり、黒い便が出る、尿に血が混じって、紅茶のような色になる
・月経過多、生理が止まりにくい
ただし、いずれの症状もこの疾患に特異的なものではありません。
■ 血小板減少症の主な治療法とは?
血小板に対する自己抗体ができ、この自己抗体により脾臓で血小板が破壊されるために、血小板の数が減ってしまうと推定されています。しかしながら、なぜ自己抗体ができるのかについては、未だはっきりとしたことはわかっていないのが現状です。主な治療は、ピロリ菌保持者には除菌を行ない、それ以外はステロイドを服用します。重症の場合は、脾臓摘出で6割が改善します。近年では、新しいTPO受容体作動薬が認可され、治療の選択が広がっています。
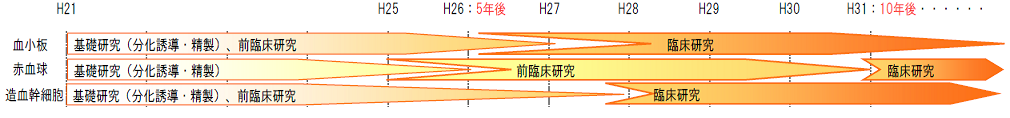
■ 再生医療/iPS細胞による血小板減少症の治療
iPS 細胞から作製する血小板の臨床応用について、「安全性確保のハードルは低いが、大量生産技術の確立が大きな課題」だと言われています。京大の江藤浩之氏らの研究グループは、ヒトiPS細胞から血小板を作製することに成功し、2011年には不死化して増殖を続ける巨核球株を得て凍結保存も可能としました。そもそものスタートとなるiPS細胞についても、血小板生産に適したものの選別法にもめどをつけ、生産の効率化に向けた研究を進めています。
そもそも再生不良性貧血や血小板減少症では、血小板製剤の輸血が繰り返し必要になるが、血小板は凍結や冷凍保存ができない。そのため、安定供給は解決策が見いだせないことが最大の課題でした。もしもiPS細胞による血小板生産システムが作れれば、現行の血液バンクを補完できると期待されています。現在、患者本人の細胞からiPS細胞を作製し、それから誘導した血小板を投与するという臨床研究の検討に着手しています。対象と想定しているのは、血小板輸血を繰り返し必要とするが、HLA型や血小板抗原の不適合などにより輸血に最適な血小板の確保が難しく困っている患者です。
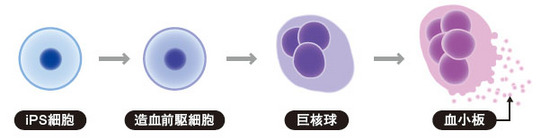 血小板は巨核球の細胞質がちぎれてできるので核がありません。そのため患者に移植した場合も腫瘍化のリスクをほぼ無視できるという、他の組織や細胞と比べてアドバンテージがあります。分化や培養の過程で血小板以外の細胞が混入しても、投与前に放射線照射で殺すことができるのです。
血小板は巨核球の細胞質がちぎれてできるので核がありません。そのため患者に移植した場合も腫瘍化のリスクをほぼ無視できるという、他の組織や細胞と比べてアドバンテージがあります。分化や培養の過程で血小板以外の細胞が混入しても、投与前に放射線照射で殺すことができるのです。
ヒトiPS細胞から作製した血小板の安全性と有効性はマウスでは検証済みなので、今後数年で、ウサギなどでも安全性と有効性を検証し、順調に進めば4~5年後には患者への投与を始める見込みです。安全性確保のハードルが低いことは利点ですが、投与が繰り返し必要となることが難点だとされており、血液バンクの補完という位置付けの規模での実用化となると、患者本人のiPS細胞からその都度作るという手法ではまず追いつきません。そこで、今後構築される予定のiPS細胞バンクとも連携し、HLA型が異なる複数の種類の血小板を大量生産できるシステムの確立が必要となります。臨床研究の準備と並行して、生産技術の効率化に向けた研究とともに、薬事法に法った開発を進めるため、企業との連携の道も探ってかなければなりません。
iPS細胞から作製した細胞や組織を臨床で使おうとする場合、問題となるのは腫瘍化などのリスクをいかに低くできるか。その点で、いち早く臨床研究のスタートが見込まれるのは加齢黄斑変性に対する網膜色素上皮細胞の移植ですが、iPS細胞から血小板製剤を作る技術も早期の実用化が有望視されています。
■ 脊髄損傷に関する再生医療/iPS細胞の最新研究成果
| 再生医療適応症 | 作成する細胞 | 主要な研究機関 | 基本情報 | 研究の進捗状況 | 最新ニュース | ||||||
| 血小板減少症 | 血小板細胞 | ・東大医科学研究所 |  |
||||||||
|
|||||||||||
|
東京大の中内啓光教授らは、様々な細胞に成長できる人のiPS細胞から、血液のもとになる「造血幹細胞」を作製することに成功しています。また、マウスにこの造血幹細胞を移植すると、幹細胞が骨髄に移動し正常に血液を作り始めることも確認されていおり、遺伝性の血液疾患マウスへの遺伝子治療にも成功しています。これまで、iPS細胞から血液細胞を試験管で作る研究は多くありましたが、きちんと機能し、移植に使うことのできる造血幹細胞を作ることは成功していませんでした。この治療方法は、ドナー不足が問題になっている骨髄移植に代わる白血病の新たな治療法開発などの足がかりになると考えられています。 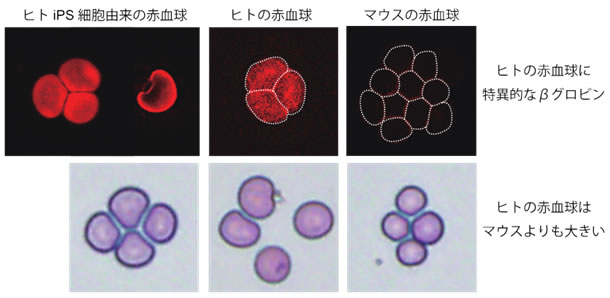
しかし残念ながら、今回の手法をヒトにそのまま応用するのは倫理面などから課題があり、今後治療に生かす際には、ブタなどで大量に造血幹細胞を作る技術などが必要となります。このため当面は、血液の難病患者などのiPS細胞を使って造血幹細胞を作り、病気の発症の仕組みや治療法の研究に役立てられます。
現在、米国のバイオベンチャーがiPS細胞から作った血小板を、血小板減少症の患者に投与する臨床試験を米食品医薬品局(FDA)に申請するなど、世界中の大学の研究グループや企業が、臨床研究の実施を目指しています。国内では、京大iPS細胞研究所の江藤浩之教授らが、既にiPS細胞から血小板を作ることに成功しています。血小板は、他の組織と違って体内で増殖せず寿命も限られるため安全性が高いと考えられ、早期の臨床研究の開始されることが見込まれています。日本でも、iPS細胞由来の血小板を活用した治療の実用化を目指して設立されたベンチャー企業であるメガカリオンも2018年頃の実用化を目指しています。
現在のところ、ヒトiPS細胞から造血幹細胞が作製できたこと、また、それを利用した遺伝子矯正治療モデルに成功したことは、将来的にこの方法によりヒトの遺伝性を含む各種血液疾患の根治的治療に役立つ可能性を秘めています。実際に遺伝子の突然変異によって正常な血液細胞が作れなくなり、免疫不全症、慢性肉芽腫症、血小板や赤血球の異常症などに苦しむ患者が大勢います。例えばその患者の皮膚からiPS細胞を作り、変異してしまった遺伝子を正常なものに治療します。この正常化したiPS細胞から動物の体内で誘導した造血幹細胞を取り出し、患者自身に移植することで病気を根治的に治療することが可能になります。
|
|||||||||||
(参考資料)
公益財団法人 難病医学研究財団/難病情報センター http://www.nanbyou.or.jp/entry/157